“Pierwsza terapia genowa w okulistyce zatwierdzona przez FDA.”
W grudniu 2017 roku FDA (Food and Drug Administration) dopuściło do obrotu preparat zawierający wirus AAV2, który przenosi prawidłowe allele genu RPE65. Jest to początek ery terapii genowej w okulistyce. Lek o nazwie Luxturna (voritogene), produkowany przez Spark Therapeutics, jest wskazany u pacjentów cierpiących z powodu dystrofii siatkówki związanej z mutacją genu RPE65. Stosuje się go na razie jedynie u osób, które posiadają mutacje w obu allelach tego genu.
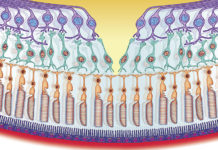
Gen RPE65 koduje enzym produkowany w komórkach nabłonka barwnikowego kluczowy dla prawidłowego przebiegu fototrandsukcji, a dokładnie regeneracji 11-cis-retinolu biorącego udział w odtwarzaniu barwników światłoczułych w fotoreceptorach. Jego mutacje są przyczyną wrodzonej ślepoty Lebera i zwyrodnienia barwnikowego siatkówki o dziedziczeniu autosomalnie recesywnym.
Luxturna (voritogene) jest obecnie jedynym dostępnym leczeniem tych schorzeń. Dostarcza do komórek nabłonka barwnikowego prawidłowe kopie genu RPE65. Voritogene podaje się w trakcie witrektomii w postaci iniekcji podsiatkówkowej, dzieciom powyżej 1 roku życia. Minimalny odstęp pomiędzy iniekcjami oka prawego i lewego to 6 dni. Na 3 dni przed iniekcją konieczne jest rozpoczęcie doustnej terapii kortykosteroidami w dawce 1mg/kg masy ciała, nie przekraczając dawki maksymalnej 40mg/dziennie.
Nowa terapia wykazała skuteczność, trwałość i bezpieczeństwo w badaniach klinicznych. Jej zastosowanie powoduje nie tylko zatrzymanie progresji choroby, ale także poprawę ostrości wzroku u badanych, która utrzymuje się w dotychczas 3–letniej obserwacji (mierzonej przez MLMT score).
Powikłaniami terapii mogą być: przedarcia siatkówki, przejściowe podwyższone ciśnienie wewnątrzgałkowe, zaćma, depozyty śródsiatkówkowe i zanik struktur w dołeczku. Z powodu techniki podania po iniekcji występuje chwilowy spadek ostrości wzroku. Następuje również przejściowy światłowstręt spowodowany polepszeniem działania pręcików.
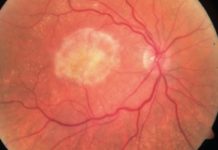
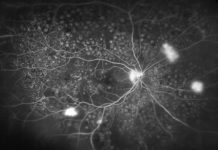
Podstawą kwalifikacji do leczenia jest obraz dna oka oraz badania genetyczne. Terapia nie jest skuteczna u pacjentów, u których nastąpiła znacznego stopnia atrofia komórek nabłonka barwnikowego oraz chorych na dystrofie nie związane z mutacją w genie RPE65. Kluczowym jest szybkie i dokładne postawienie diagnozy.
Luxturna będzie dostępna w USA już w marcu 2018 r. Niestety na razie ogromną wadą leku jest jego cena – 425 tys. dolarów za jedną iniekcję. Jednakże niewątpliwie jest to przełom w terapii schorzeń genetycznie uwarunkowanych w okulistyce.
Na podstawie: Cheryl Guttman Krader, Alex V. Levin, Paulo Falabella, FDA approval of retinal dystrophy drug launches era of ocular gene therapy, Modern Retina, Luty 2018.